概要
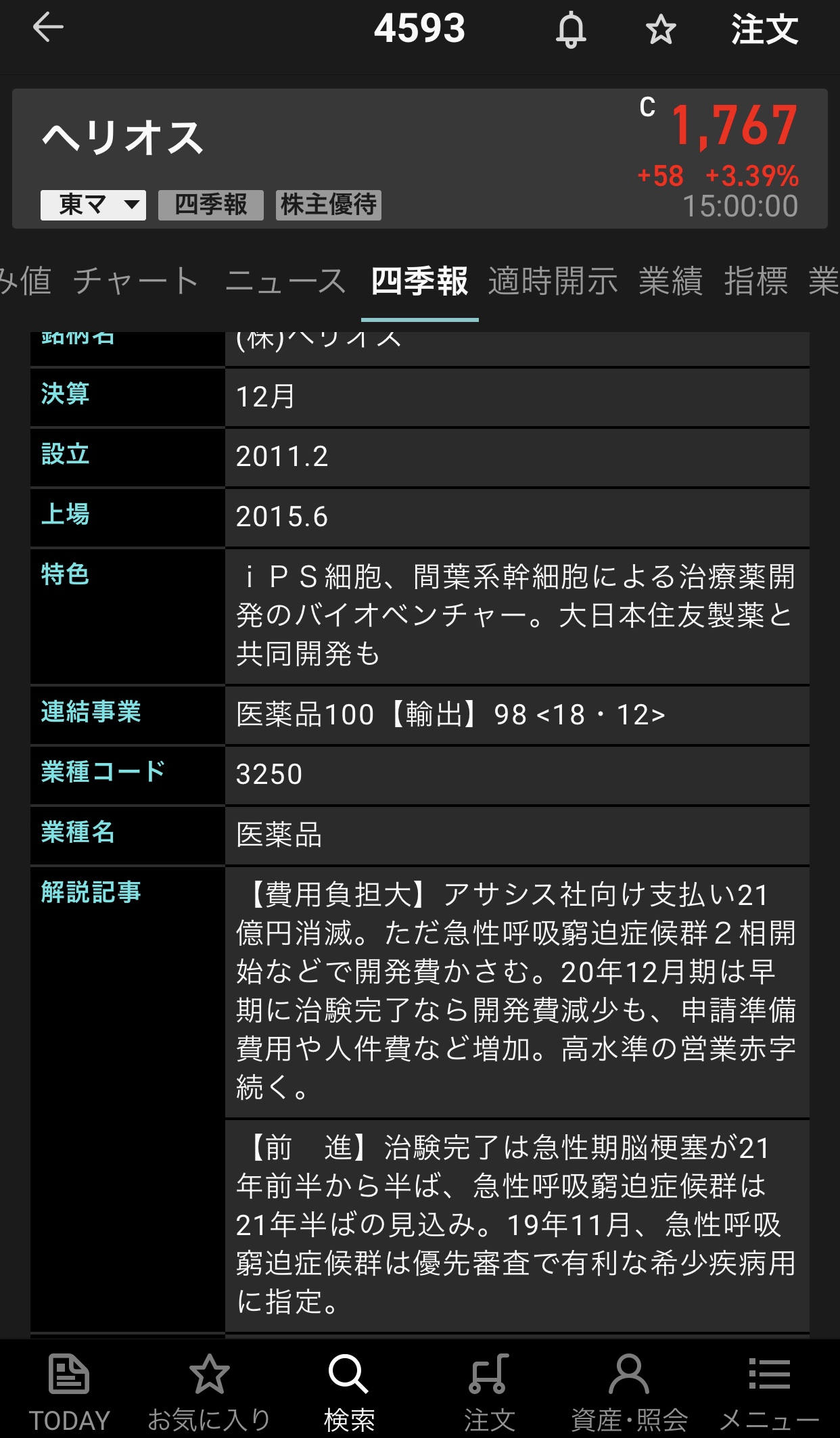
当社は現在、米国 Athersys, Inc(以下、アサシス社と言います。)の創製した幹細胞製品 HLCM051(MultiStem®) を用いて、日本国内において急性呼吸窮迫症候群(ARDS) を対象疾患とした治験(治験名: ONE-BRIDGE 試験)※3 と脳梗塞を対象疾患とした治験をそれぞれ実施しております。
方、欧米においては、アサシス社が同製品を用いた ARDS 患者に対する第Ⅰ/Ⅱ相臨床試験(治験名:MUST-ARDS 試験)を完了し、2019 年1月にはその速報にて、投与後 28 日後における評価において、ポジティブな結果が得られた事を発表しております。また、その後、2019 年5月に開催されました AmericanThoracic Society International Conference(ATS、米国胸部学会)での MUST-ARDS 試験の治験責任医師である Dr. Geoff Bellingan による発表では、MultiStem 投与群及び非投与群における炎症性サイトカインの反応の差などが示され、MultiStem の一貫した免疫調整という薬理作用に関する理解が深まりました。
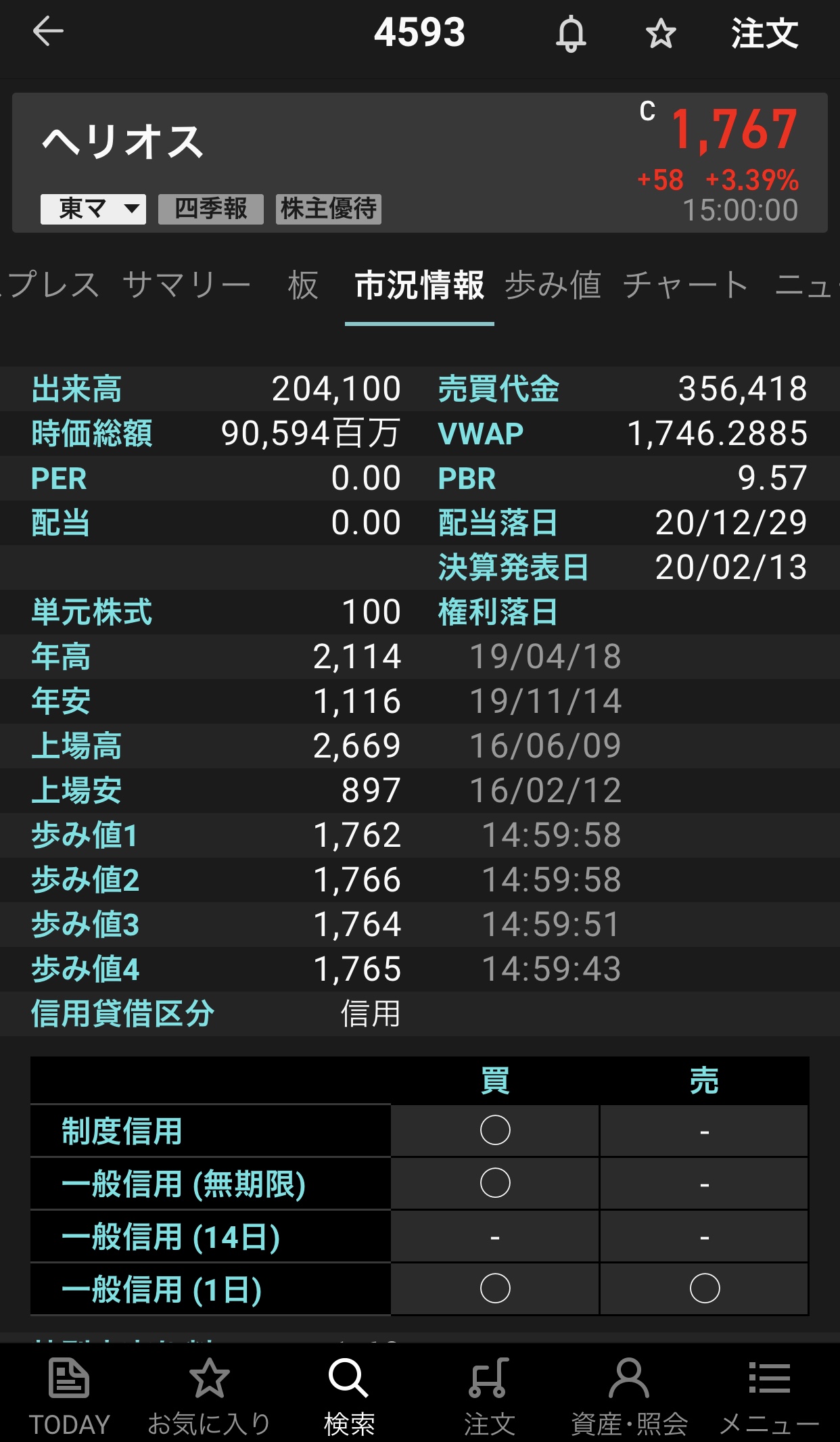
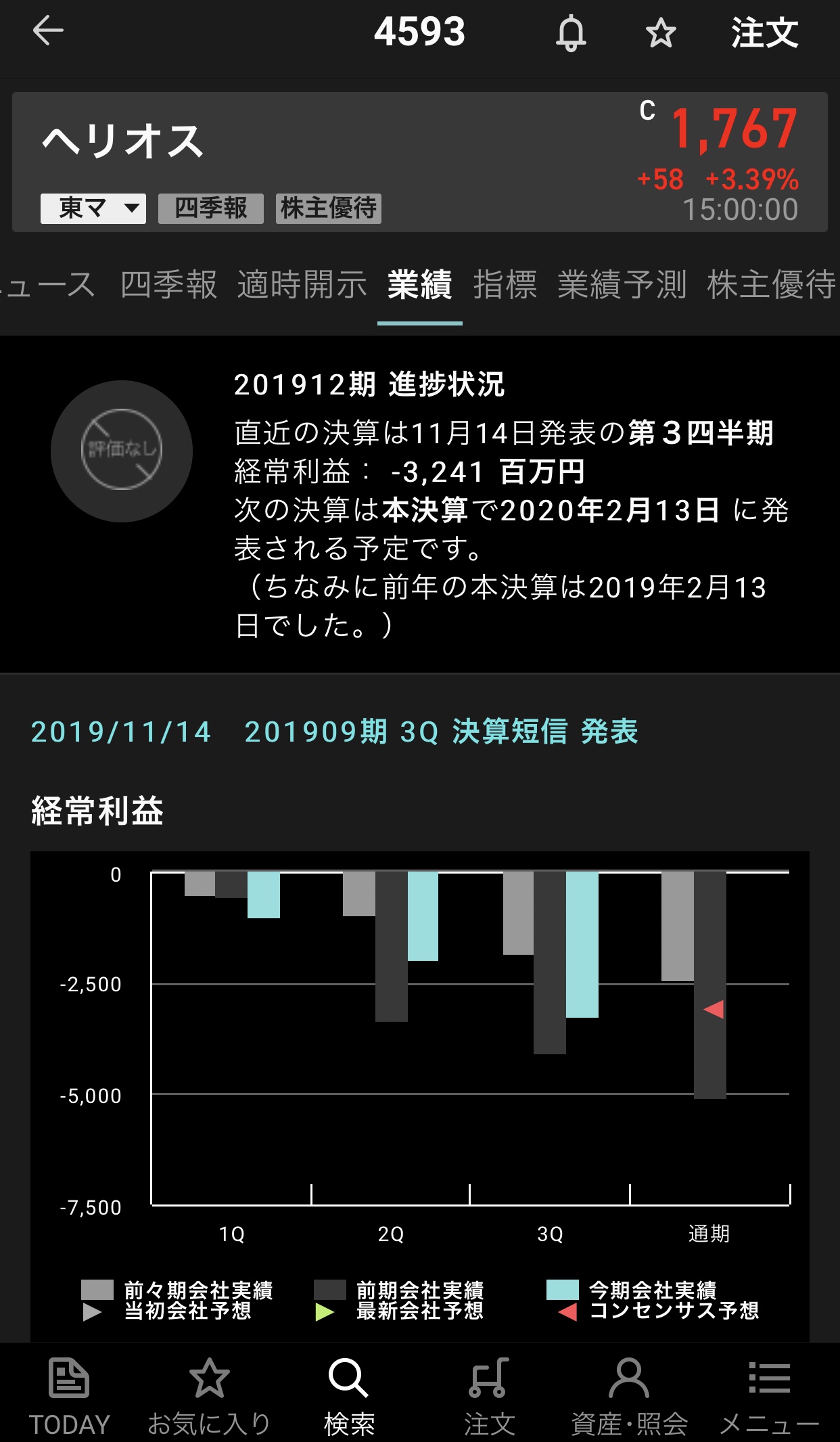
ヘリオス【4593】の情報